Présentation
Les paraparésies spastiques héréditaires (PSH) sont caractérisées par l’apparition, chez l’enfant ou l’adulte, d’une atteinte motrice (spasticité, syndrome pyramidal, faiblesse) et sensitive profonde des membres inférieurs.
Il existe un gène majeur : SPG4 (environ 15-20% des formes sporadiques, 40% des formes dominantes), suivis par d’autres gènes relativement fréquents (dominants : SPG30, SPG3A, SPG10, SPG31; récessifs SPG7, SPG11, SPG5, SACS, SPG8, SPG30). Les CNV sont un mécanisme mutationnel fréquent dans les PSH (10-25% des mutations de SPG4) et ne sont actuellement pas bien détectés en séquençage très haut débit (STHD)1.
Au delà de SPG4 (et des gènes les plus fréquents), les bases moléculaires des PSH sont nombreuses et hétérogènes, encore mal connues, avec à ce jour plus de 100 gènes impliqués, menant à des chevauchements avec d’autres catégories syndromiques (ataxies, leucodystrophies, syndromes parkinsoniens, NBIA, neuropathies…) et pour lesquelles le STHD présente une réel intérêt.
1 Ces 10 Gènes les plus fréquents rendent 85% des diagnostics (Banneau, Méreaux et al, en cours de publication). La stratégie sera susceptible d’être modifiée en fonction de l’amélioration de la détection des CNV en STHD et de l’activation de toutes les RCP d’aval.
Critères avant d'envisager une discussion en RCP
Pas de STHD proposé pour l’instant pour :
- Cas sporadique, début > 50 ans
Cas sporadique de début <50 ans ou cas familial :
- Examen clinique complet
- IRM cérébrale avec séquence T2*/SWI et sagittales T1, à compléter avec un scanner cérébral si doute sur des dépôts de Fer/calcium
- IRM médullaire
- Sauf si forme familiale clairement dominante :
- Biomarqueurs 1 : AGTLC à jeun, Homocystéine, cholestanol, acide phytanique, acide pristanique, 25-27 hydroxycholestérol
- Panel des gènes les plus fréquents avec analyse des CNV1
(!) Si une ataxie est associée, penser aux pathologies à expansion (SCA pour les formes dominantes, Friedreich pour les formes récessives)
Envoi en duos au minimum, en trios si possible
- Prélever ≥ 1 autre atteint (tous ceux disponibles, privilégier les atteints éloignés) et/ou
- Prélever ≥ 1 parent sain :
- Cas sporadique : les deux parents si possible
- Apparenté sain (cousin premier degré..) : privilégier la branche « non à risque » ;
- Apparenté sain mais à risque : privilégier ceux d’âge > à l’âge de début de la pathologie chez le cas index
(!) Pénétrance incomplète et expressivité variable des pathologies, attention au diagnostic présymptomatique non souhaité
- Prélèvement « en Solo » autorisé en exception : si début pathologie <20 ans ou cadre familial clair (≥2 atteints, consanguinité )
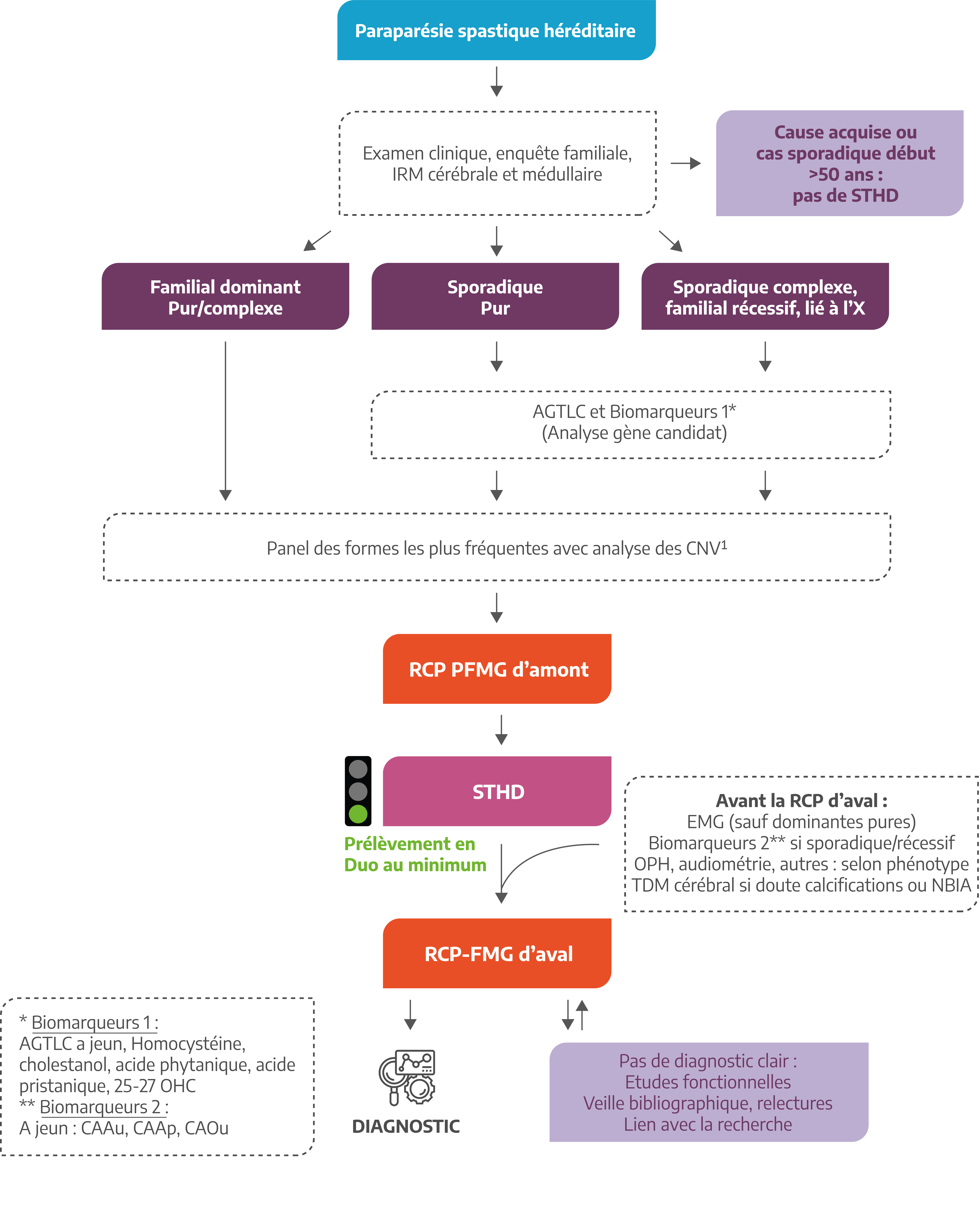
Place du STHD dans la stratégie diagnostique
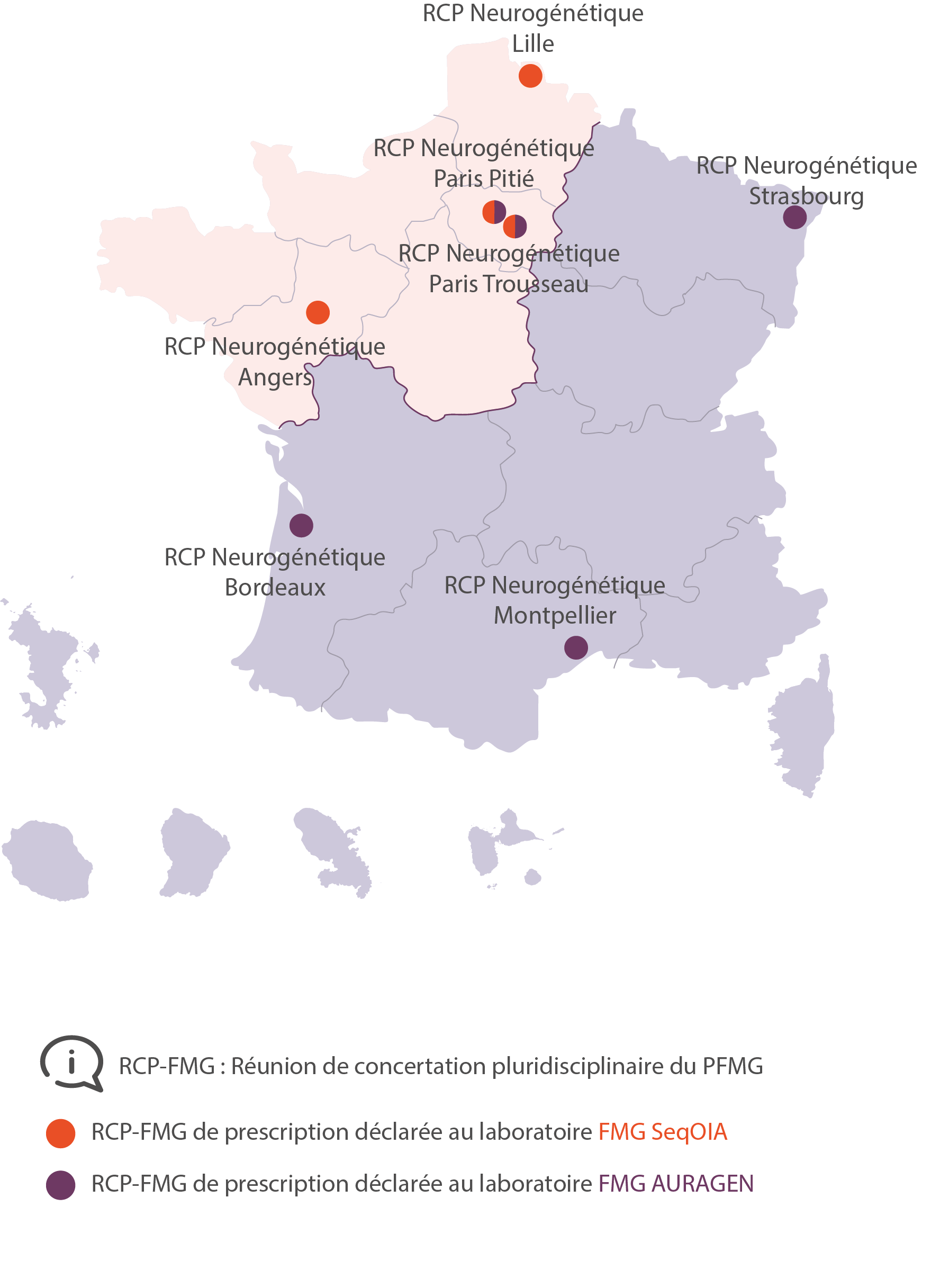
RCP Neurogénétique Paris Pitié
Claire EWENCZYK
Alexandra DURR
Perrine CHARLES
Anna HEINZMANN
RCP Neurogénétique Paris Trousseau
RCP Neurogénétique Angers
RCP Neurogénétique Bordeaux
Cyril GOIZET
RCP Neurogénétique Strasbourg
Mathieu ANHEIM
mathieu.anheim@chru-strasbourg.fr
Christine TRANCHANT
christine.tranchant@chru-strasbourg.fr
Solène FRISMAND
Matthieu BEREAU
Christel THAUVIN
Anne DOE DE MAINDREVILLE
adoedemaindreville@chu-reims.fr
Juliette Piard
RCP Neurogénétique Montpellier
RCP Neurogénétique Lille
David DEVOS
Luc DEFEBVRE
Sylvie NGUYEN-THETICH
sylvie.nguyenthetich@chru-lille.fr
Gaël NICOLAS
Eugénie MUTEZ