Monsieur P., 47 ans, sans antécédents significatifs, est porteur d’un rhabdomyosarcome pléomorphe rétropéritonéal métastatique pulmonaire (stade IVB) depuis mars 2019.
En échappement thérapeutique après 3 lignes de traitement, il a d’abord reçu une chimiothérapie cytotoxique (doxorubicine et ifosfamide, 6 cures) avec une maladie stable puis une irradiation de la tumeur primaire en septembre 2019. Les sites métastatiques pulmonaires progressent ; Monsieur P. reçoit alors du pazopanib, une thérapie ciblée anti-angiogénique, stabilisant la maladie durant 6 mois, suivi de 6 mois de progression lente. En avril 2021, il reçoit une 3e ligne de traitement par VIT pour 3 cures, avec une tolérance médiocre et une progression immédiate.
Monsieur P. a bénéficié d’un RNAseq ciblé en 2019, n’ayant aucun impact théranostique et confirmant le diagnostic. Il a bénéficié d’un screening immunologique pour les protocoles CONGRATS, mais il n’était pas incluable.
L’analyse moléculaire effectuée sur AURAGEN en juin 2021 a permis de mettre en évidence une mutation inactivatrice de NF1, non identifiée par l’analyse effectuée sur le panel de gènes.
Sur cette base, il est inclus dans le programme de recherche clinique COTESARC, étude multicentrique prospective promue par le Centre Léon Bérard. Il reçoit alors l’association du cobimetinib, un inhibiteur de MEK agissant sur la voie oncogénique activée par la perte de NF1 et de l’atezolizumab, une immunothérapieanti-PDL1. Notons que les analyses tumorales effectuées précédemment sur l’analyse du protocole CONGRATS (absence de structure lymphoïde tertiaire) suggéraient un risque majeur de progression précoce sous immunothérapie seule (Petitprez et al, Nature 2020).
Après 5 mois de traitement, l’étude rapporte une amélioration symptomatique franche du patient, avec disparition des douleurs abdominales et une réponse volumétrique sur les métastases pulmonaires (cf. figure). La masse tumorale volumineuse abdominale est stable alors qu’elle était progressive à 2 mois avec le traitement précédent. Les effets secondaires sont modestes : une asthénie de grade 1 et une anémie de grade II. Monsieur P. poursuit son traitement au 07/12/2021.
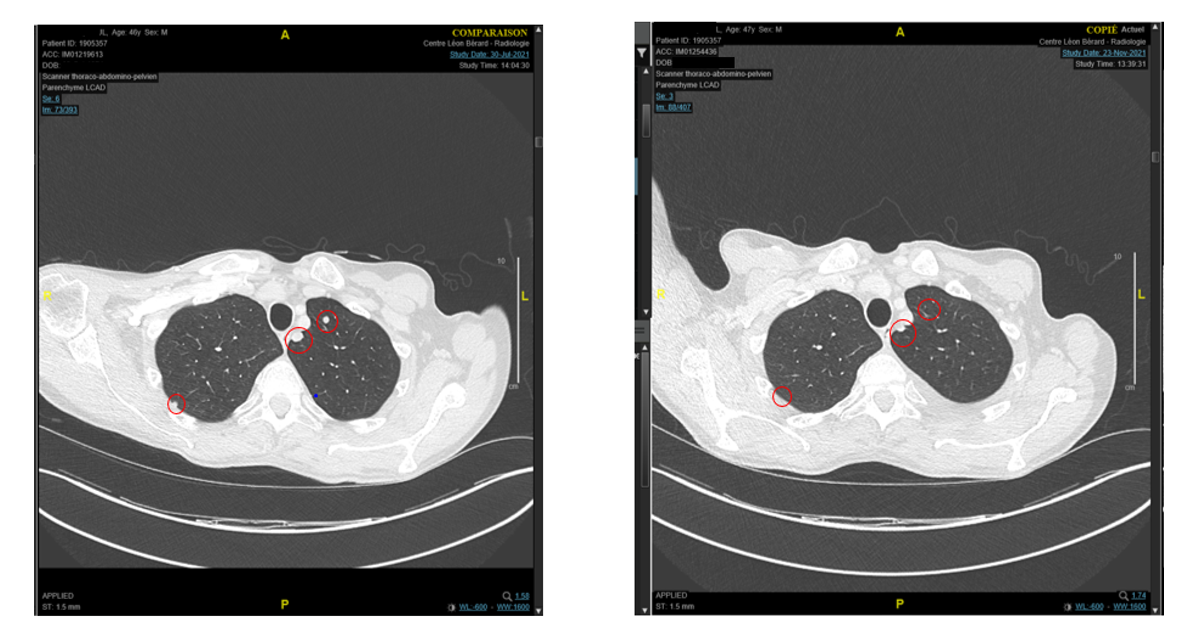
Figure : scanners thoraciques au 30 juillet 2021 (à gauche) et au 23 novembre 2021 (à droite) : la régression tumorale est estimée à 25% sur les lésions cibles pulmonaires.
Ce traitement n’aurait pas été mis en place sans l’analyse moléculaire effectuée dans le cadre du PFMG2025.
NB : Monsieur P. n’était pas incluable dans l’étude clinique MULTISARC.

